
La flora intestinal forma un ecosistema en sí mismo. Uno que influye en la salud y en el estado de ánimo de su huésped: nosotros, los humanos.
El estudio de los microorganismos que pueblan el intestino de los animales, incluidos los seres humanos, es una disciplina en crecimiento. Las funciones del llamado microbioma intestinal van mucho más allá de ayudarnos a hacer bien la digestión. Influye en nuestro sistema inmune, se comunica con nuestro cerebro y puede incluso relacionarse con la respuesta de nuestro cuerpo a la COVID-19.
Yolanda Sanz, doctora en farmacia e investigadora del Instituto de Agroquímica y Tecnología de Alimentos (IATA) del CSIC, es una de las referencias europeas a la hora de estudiar la relación entre la ecología de nuestros microbios intestinales, la nutrición y la salud. Entre otros éxitos, su equipo ha patentado una bacteria que podría funcionar como antidepresivo.
– Ahora que nuestras vidas están controladas por un virus, ¿deberíamos empezar a prestarles más atención a los microbios que han colonizado nuestro intestino?
Es un buen momento para planteárnoslo, aunque las investigaciones sobre estos microorganismos que viven con nosotros vienen haciéndose desde hace al menos dos décadas. Sabemos que desempeñan funciones muy importantes para el funcionamiento de nuestro cuerpo. No solo gastrointestinales, sino todo tipo de funciones metabólicas. También estamos descubriendo conexiones con el cerebro.
Ahora mismo, nos estamos centrando en cómo estos microorganismos activan nuestras defensas contra las infecciones. Con respecto a la COVID-19, hemos empezado a encontrar evidencias también de que la microbiota de nuestro intestino puede tanto influir en la respuesta inmunológica de nuestro organismo como agravar la inflamación que se produce en los casos más severos.
«La gran colonización del intestino se produce en la infancia, cuando el recién nacido entra en contacto con el medio externo»
– Desde fuera tendemos a ver nuestro cuerpo como algo estanco, protegido del exterior, pero, ¿cuántos microorganismos forman la microbiota intestinal de una persona sana?
Es difícil hacer estimaciones, no los podemos contar a mano. Además, su concentración varía en función de la zona del aparato digestivo. En el estómago la carga es baja, unos 10 000 por gramo de tejido intestinal. En la parte alta del intestino tenemos ya entre uno y diez millones. Y en el colón tenemos la población más alta, entre uno y 100 billones de microorganismos.
Inicialmente, se decía que teníamos 10 veces más microorganismos que células humanas. Pero las estimaciones actuales hablan de una relación de uno a uno. Tenemos tantos microbios como células en nuestro cuerpo.
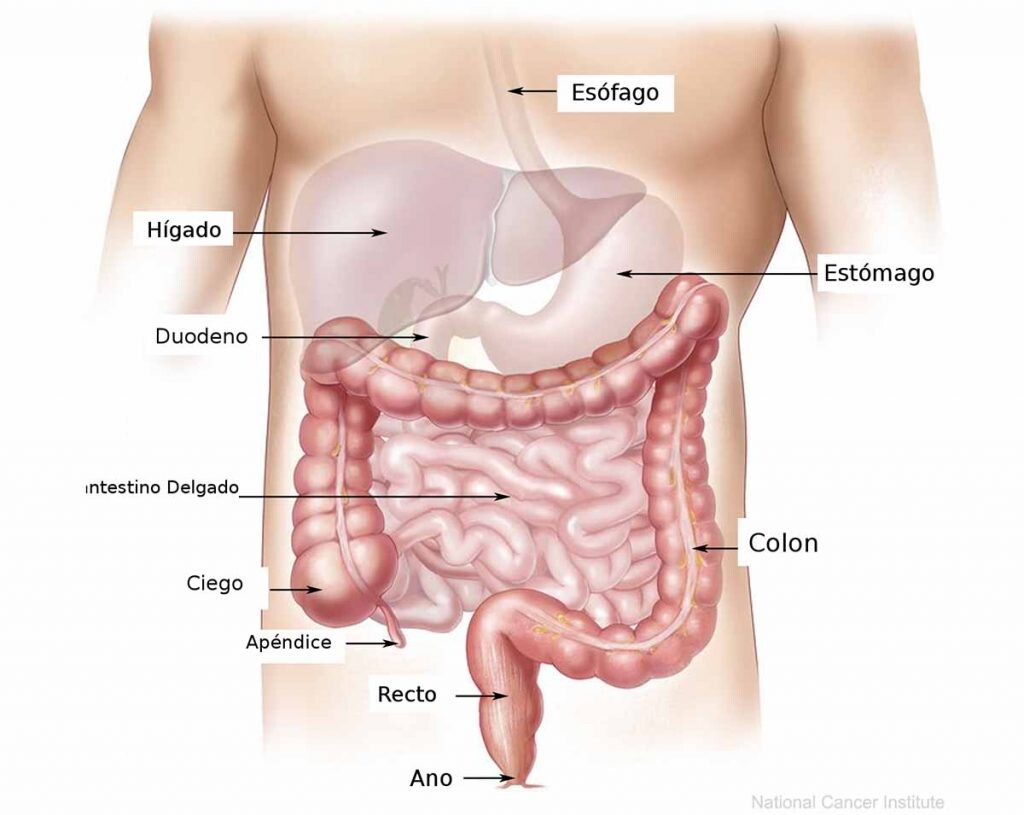
– ¿De qué tipo de microorganismos hablamos?
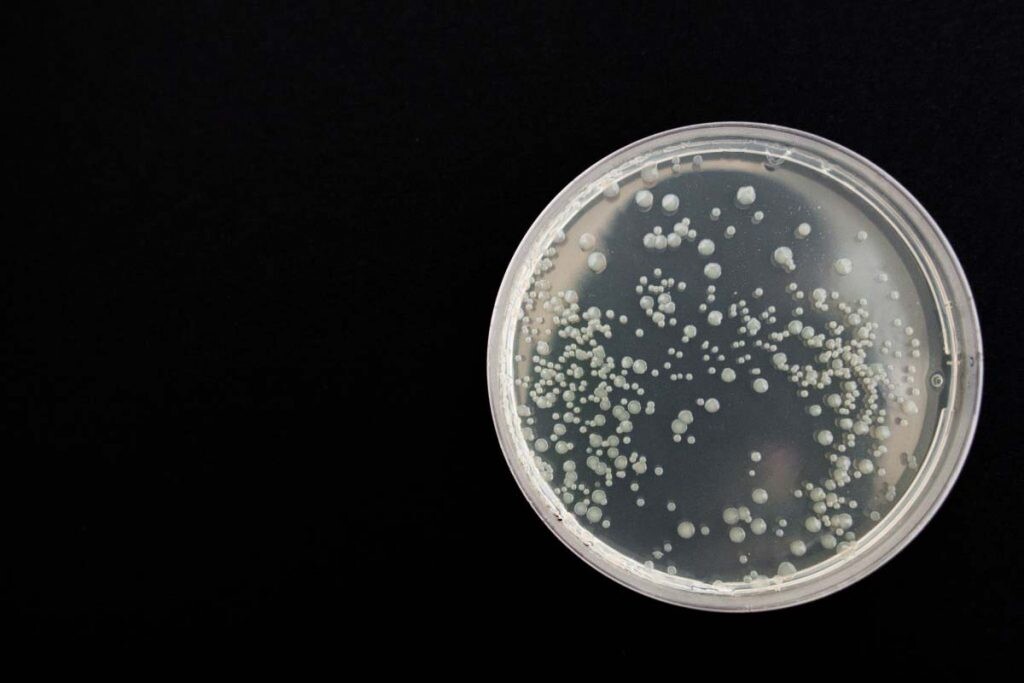
Tenemos todo tipo de organismos. Se conocen más de 1000 especies distintas. Tenemos virus, bacterias, arqueas… El 90% se estima que son bacterias, que es donde se centra también nuestra investigación. Queremos entender bien sus funciones, tanto de forma individual como colectivamente. Estamos hablando de un ecosistema en el que los microorganismos interaccionan entre sí, con el medioambiente y con el organismo hospedador, nosotros.
– El genoma humano contiene más de 23 000 genes, mientras que nuestro microbioma se compone de más de tres millones de genes. ¿Somos más bacteria que humanos?
Desde el punto de vista genético, somos más bacteria que humano. La capacidad de codificar proteínas de la microbiota es entre 100 y 150 veces superior a la de nuestro organismo.
– ¿Cuánto sabemos de ellos? ¿Hay especies desconocidas?
Nos faltan por descubrir especies, eso es seguro. Ahora mismo, desde la biología molecular, identificamos microorganismos en base a su secuencia genética, a trozos de ADN. Pero para caracterizar bien una especie hay que cultivarla en laboratorio, estudiarla de forma individual. Es decir, nos faltan técnicas para poder estudiar la bacteria completa en laboratorio y no solo un trozo de un gen.
– ¿Cómo llegan todos esos microorganismos a nuestro intestino?
Aunque hay contactos con microorganismos antes de nacer, la gran colonización se produce en la infancia, cuando el recién nacido entra en contacto con el medio externo. Hay muchos factores que influyen en el tipo de microbioma: el tipo de parto y de lactancia, el uso de antibióticos, si hay animales en casa, si hay más o menos hermanos…
Cuando empiezan a incorporarse los alimentos sólidos a la dieta, se produce una revolución. La microbiota se diversifica en especies. Los microorganismos se adaptan y empiezan a predominar aquellos que son capaces de digerir lo que comemos. Cuanto más variada es nuestra dieta, más diverso el microbioma. En torno a los dos o tres años este ecosistema se estabiliza.
«Tener una dieta variada multiplica las competencias biológicas de las bacterias, les da estabilidad y permite que hagan frente a cualquier situación o cambio en el ecosistema»
– ¿Qué elementos influyen en el estado de la microbiota intestinal?
La dieta es uno de los factores más importantes. Pero también influyen el uso de medicamentos. Por ejemplo, además de los antibióticos, los inhibidores de la bomba de protones [los antiácidos] influyen en la composición de la microbiota. Los psicofármacos o la metformina para la diabetes también se ha descubierto que tienen un impacto en los microorganismos intestinales.
– ¿Cómo debería ser nuestra dieta para mantener una flora intestinal sana?
Las recomendaciones sobre dieta siempre deben hacerse de forma personalizada. Cada uno tiene una microbiota diferente. Cada persona responde de forma distinta a los alimentos. Aun así, en general, puede concluirse que la variedad de la dieta ayuda a tener una microbiota más diversa. La diversidad, a su vez, multiplica las competencias biológicas de las bacterias, les da estabilidad y permite que hagan frente a cualquier situación o cambio en el ecosistema.
Además de la biodiversidad, una dieta rica en fibra, que es la principal fuente de carbono de nuestras bacterias comensales, es beneficiosa. Si tuviese que darse un mensaje genérico, sería: variedad y riqueza en fibra.

– ¿Cómo influye la salud del microbioma en nuestro día a día?
Lo hace a través de muchas funciones. Una de las que más hemos estudiado es su influencia en el sistema inmunitario. De forma directa, los microorganismos, aunque sean beneficiosos, estimulan el sistema de defensa. La colonización del intestino del recién nacido hace que madure su sistema inmunológico. Sirve de entrenamiento para reconocer qué cosas son dañinas y qué cosas son inocuas. Es decir, nuestro cuerpo aprende a ser capaz de mantener la microbiota intestinal y, al mismo tiempo, reconocer las bacterias y virus patógenos.
– Esto está relacionado con otro de vuestros campos de estudio: la influencia del microbioma en la respuesta inmune a la COVID-19.
Es una línea de investigación que empezamos el pasado verano. Uno de los proyectos busca evaluar cómo cambia la microbiota en pacientes COVID positivos, comparándolos también con pacientes oncológicos. Queremos comprender si la microbiota tiene que ver con la severidad de la infección y si influye en la respuesta inmunológica del paciente infectado.
El otro proyecto, que empezamos en agosto, busca evaluar si la microbiota de los niños en edad escolar tiene que ver con que sean más o menos susceptibles a la infección. Estamos muestreando a niños sanos y los convivientes de la unidad familiar.
Ninguno de estos proyectos está concluido, ya que se necesitan estudios con poblaciones muy grandes para poder sacar conclusiones. Esperamos poder empezar a extraer las primeras conclusiones en febrero o marzo.
«Por primera vez en humanos se ha demostrado que hay una conexión entre el intestino y el cerebro»
– Uno de los últimos grandes proyectos de investigación sobre el microbioma intestinal fue MyNewGut. Entre sus conclusiones principales, se señalaba que la microbiota influía en la obesidad. ¿De qué manera?
Por un lado, hemos comprobado que el microbioma influye en la conexión intestino-cerebro. Para probarlo, hicimos trasplantes fecales de personas sanas a personas enfermas, con síndrome metabólico. Vimos que el cambio de microbiota influía en el sistema nervioso central y en el cerebro, y lo hacía en procesos que tienen que ver con el control de la ingesta. Los individuos con microbiomas más saludables la controlaban mejor.
Por primera vez en humanos se ha demostrado que hay una conexión entre el intestino y el cerebro; y que una microbiota más sana puede ayudarnos a controlar mejor la cantidad de energía que ingerimos. La relación con la obesidad es clara.
Además, también hemos descubierto que hay bacterias con efectos concretos. Hay una que tiene efectos antidiabéticos y otra que ayuda a potenciar las defensas del intestino frente a dietas ricas en grasa que, sostenidas en el tiempo, suelen causar inflamación.
– ¿Este eje intestino-cerebro influye también en otras enfermedades?
Ahora mismo formamos parte de un proyecto europeo, EarlyCause, en el que investigamos cómo el estrés en edades tempranas puede aumentar el riesgo de desarrollar depresión y patologías cardiacas y metabólicas asociadas. Esto tiene también una relación directa con el eje intestino-cerebro.
El estrés es una reacción normal que genera una sustancia llamada glucocorticoides que nos ayudan a reaccionar rápido, a movilizar nuestras reservas de energía. Al mismo tiempo, generan una respuesta antiinflamatoria, para que el cuerpo no sufra. Pero si el estrés es crónico y sostenido, se produce una resistencia a los glucocorticoides y una inflamación crónica.
Por resumir, el estrés crónico afecta al microbioma y este a su vez puede generar trastornos a largo plazo. Aumenta nuestra vulnerabilidad y nos predispone a sufrir otras enfermedades. En este sentido, hemos patentado una bacteria, Christensenella minuta, que puede servir para tratar los trastornos del estado de ánimo, como la depresión y la ansiedad.
– Hablamos de conexión entre los microbios del intestino y el cerebro humano, pero, ¿cómo se comunican?
Lo hacen de varias maneras. Por un lado, los microorganismos producen sustancias que pueden penetrar la barrera hematoencefálica que rodea el sistema nervioso. Y por otro, sabemos que la microbiota intestinal influye en la generación de neurotransmisores [moléculas que permiten la transmisión de información de las neuronas a otras células]. Por ejemplo, un 90% de la serotonina, que nos ayuda a regular nuestras emociones, se produce en el intestino.
– ¿Podría llegar a hacerse un ‘trasplante’ de microbiota para curar enfermedades?
El trasplante fecal, para reemplazar la microbiota del paciente, se está usando en casos concretos de infección por Clostridium difficile que ya no responden a los tratamientos habituales. Es un último recurso.
A nivel experimental, se está probando para otro tipo de enfermedades. Hay unos 170 ensayos en marcha. Por ahora, sin embargo, no se considera un tratamiento ideal por muchas razonas. Es muy difícil seleccionar a los donantes y definir si tienen una microbiota sana. Además, estás transfiriendo material biológico del que no se conoce su composición al 100%. Conlleva una serie de riesgos difícilmente subsanables. También se ha observado que en algunos casos funciona muy bien y en otros el trasplante no funciona. En conclusión, es algo muy difícil de estandarizar.
Creo que hay que avanzar hacia las microbiotas sintéticas. Es decir, poder seleccionar las bacterias que sabemos que sí son beneficiosas, combinarlas de forma controlada, comprobar su seguridad… De esta manera podría llegar a convertirse en una terapia reproducible, con parámetros de calidad y eficacia bien establecidos, como los de otros medicamentos.
Por ahora, esto se está desarrollando con bacterias concretas. Es el futuro inmediato. A largo plazo, el reto es ser capaces de combinarlas y crear una microbiota sintética controlada.
– Conociendo cómo estos microorganismos influyen en la salud, ¿podríamos llegar a prevenir enfermedades mediante su estudio?
Nosotros pensamos que sí. Estamos estudiando cómo la microbiota de individuos sanos tiene relación con la mayor o menor incidencia de algunas enfermedades. Es lo que estamos haciendo, por ejemplo, con el estudio de los niños y la infección por coronavirus.
En Nobbot | Bacterias contra virus: una guerra milenaria con un final inesperado
Imágenes | IATA-CSIC, Wikimedia Commons, Pxhere, Mepixels, Unsplash/ja ma

Soy paciente con 11 años de tratamiento con antidepresivos . Me gustaría participar como paciente de sus estudios ya que suelo tener muchos problemas intestinales desde hacía 2 años. Saludos
Yo desde que tengo memoria alrededor de los 8 años sufro de estreñimiento con obstrucciones intestinales en varias ocasiones y crisis de hemorroides. El día de hoy tengo 56 y sufro de depresión fuerte, ansiedad y artritis reumatoide avanzada, sufro mucho. Ahora es que se viene acertando sobre esta teoría, el intestino el segundo cerebro..
Hola. Un familiar mío lleva unos 10 años peregrinando por consultas privadas y públicas sin encontrar solución alguna. Tiene diagnóstico de intolerancia a fructosa y sorbitol, colon irritable, reflujo biliar, gastritis antral, Sibo, candidiasis intestinal, ansiedad y/o crisis de pánico, alteraciones del sueño, cansancio, fuertes dolores gástricos y abdominales, eructos e inflamación crónica, dolores musculares sobre todo lumbares y dolores de articulaciones. A pesar de hacer una dieta sin gluten, sin azúcares ni alimentos procesados, su colesterol está por encima de 300 y la vitamina D por los suelos a pesar de tomar suplemento. La medicina tradicional solamente trata síntomas pero no el conjunto de toda la enfermedad y todas las especialidades implicadas por lo que es bastante desesperante vivir así.
Mi hijo de 18 lleva 4 años con dolores abdominales, problemas de estreñimiento, estancamento ponderal. Tiene un nivel de ansiedad alto debido á su condición de TEA. Hace un año tratado con antibióticos para combatir sobrecreciemento bacteriano. Vuelve a estar ahora con antibióticos por 3 meses y corticoides 6 meses por lo mismo. Su calidad de vida es penosa. Contáctennos si quieren un caso clínico. Gracias
Hola! me llamo Elena y también estoy buscando, muy interesada, como participar como paciente, en estos maravillosos nuevos enfoques. De pequeña en una época muy concreta ( 8 años a 13) fui obesa sin saber el porqué de la transformación ( medicamentos?) y viví mucho estress ,tanto a esta edad como despues. Apareció la depresión. No tolero los fármacos produciendo efectos secundarios. Me gustaria muchisimo participar o tener mas información. És importante investigar y seguir investigando. La depresión es una enfermedad terrible que sufren muchas personas y hace mucha falta ir más allá de los farmacos. Gracias y ojalá sea posible.
Hola, me gustaría probar, aunque fuera como paciente de análisis clínico. Llevo toda la vida con depresión y muchos problemas intestinales, ninguna medicación ha llegado a hacer el gran efecto deseado aunque mejoren alguna cosa. Por favor, si es posible pónganse en contacto conmigo. Muchas gracias
Me encantaría probarlo hasta como conejillo de indias,sufro ansiedad crónica y variadisimos dolores que traen con ellos la depresión. No tolero ninguna medicación continuada,me aportan muchos más problemas que soluciones pero estoy tomando